某同学进行如下两个实验。请回答有关问题:
(1)配制50g质量分数为6%的氯化钠溶液:
①配制溶液的步骤:计算、称量和量取、 、装瓶、贴标签。
②下列情况中,会导致所配溶液的溶质质量分数偏小的是 (填字母序号)。
A.氯化钠固体不纯 B.量取水时俯视读数 C.装瓶时洒出少量溶液
D.配制溶液的烧杯内壁沾有水
(2)粗盐中难溶性杂质的去除:
步骤如下:①取一定质量的粗盐样品,加水溶解;②过滤;③蒸发结晶;④称量、计算产率。在上述各步实验中,都用到的一种仪器是 ,它在步骤②中的作用是 。
根据下列实验装置图回答问题:
(1)写出标号为a的仪器名称: 。
(2)实验室制取并收集二氧化碳时,你选择的最佳装置是 (在A、B、C、D、E、F中选填),该反应的化学方程式是 。
(3)可以用E装置收集氧气的原因是 ;若采用G装置收集氧气,你怎样验满? 。
(4)若用A、E装置制取氧气,当锥形瓶内出现大量气泡时,仍收集不满,其原因可能是 。
(5)实验室常采用加热固体醋酸钠和氢氧化钠的方法制取甲烷,你所选用的发生装置是 (填字母)。该发生装置还可以制取其他气体,请你写出一个制取其他气体的化学方程式: 。
根据下列实验示意图回答问题:

(1)图A所示实验测定空气中氧气含量,可能导致的后果是 。
(2)图B所示实验探究铁锈蚀的条件,得到的实验结论是 。
(3)图C所示实验探究燃烧条件,观察到的现象是 。
(4)图D所示实验的目的是 。
(5)图E所示实验稀释浓硫酸,该实验的操作错误是 。
新能源的开发和利用是人类社会可持续发展的重要课题。氢、氧燃料电池是一种新型能源,所用的氧气从空气中获得的方法是 。空气中的氧气按体积计算,大约是空气总体积的 。氢气可用天然气制取,这种方法制取的氢气中往往混有二氧化碳和一氧化碳,为了证明混合气体中H 2、CO 2、CO三种气体都存在,一化学实验小组设计以下实验。

【阅读提示】
①实验前,装置内的空气已排尽。
②实验过程中的尾气已处理。
③无水硫酸铜是白色粉末,吸水后变蓝。
请回答下列问题。
(1)A装置的作用是 。
(2)C装置中的实验现象是 。
(3)E装置中盛放的试剂应该是 ,该装置中发生反应的化学方程式为 。
(4)证明氢气存在的实验现象是 。
(5)另一小组同学利用上述实验装置(把其中的E装置换成装有碱石灰的干燥管),仿照上述实验过程,通过定量的方法确定一氧化碳存在,记录实验数据如下:
(注:反应生成的水蒸气被D装置完全吸收,不考虑其他水蒸气对实验结果的影响)
|
实验前C装置玻璃管内固体总质量/g |
m 1 |
|
实验后C装置玻璃管内固体总质量/g |
m 2 |
|
实验前D装置总质量/g |
n 1 |
|
实验后D装置总质量/g |
n 2 |
利用如表数据,计算出能证明CO存在的质量关系是 。(用m 1、m 2、n 1、n 2表示)
实验室有失去标签的两瓶无色溶液,分别是氢氧化钡溶液和稀硫酸。为了鉴别它们设计如下鉴别方法:先把两瓶溶液分别贴上标签A、B,然后进行实验。
|
加入的试剂 |
实验现象 |
实验结论 |
|
|
方法1 |
锌粒 |
A中无明显现象 B中产生气泡 |
A是 溶液; B是 溶液 |
|
方法2 |
碳酸钠溶液 |
A中 ; B中 。 |
化学小组同学对方法2进一步探究,设计了如下实验方案
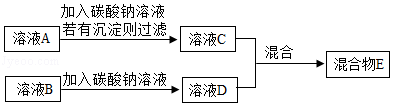
溶液C和溶液D混合,可能有以下三种情况:
(1)若有气泡产生,写出反应的化学方程式 ;
(2)若有沉淀产生,通过现象可推出溶液C中的溶质是 ;
(3)若无明显现象,混合物E中所含溶质种类最多时,写出所有溶质的化学式 。
我国制碱工业采用联合制碱法生产纯碱,其反应原理如下:
NaCl+NH 3+H 2O+CO 2═NaHCO 3↓+NH 4Cl 2NaHCO 3  Na 2CO 3+H 2O+CO 2↑
Na 2CO 3+H 2O+CO 2↑
【资料阅读】
①通常情况下,浓氨水具有较强的挥发性,易挥发出氨气。氨气是一种无色有刺激性气味的气体,极易溶于水,排放到空气中会污染空气。
②饱和碳酸氢钠溶液不能吸收二氧化碳。
化学兴趣小组在实验室模拟联合制碱法进行了如下实验:

Ⅰ.关闭K 1,先打开K 2通入NH 3,调节气流速率,待其稳定后,再打开K 1通入CO 2。
Ⅱ.待三颈烧瓶内出现较多固体时,关闭K 2停止通入NH 3;一段时间后,关闭K 1停止通入CO 2。
Ⅲ.将三颈烧瓶内反应后的混合物过滤,将滤出的固体洗涤、低温干燥,得到碳酸氢钠固体。再将其加热使其完全分解即得纯碱。
请回答下列问题。
(1)写出A装置中反应的化学方程式 。
(2)B装置中饱和碳酸氢钠溶液的作用是 。
(3)D装置中生石灰的作用是 。
(4)C装置中长颈漏斗的作用除了随时添加饱和食盐水,还有 作用。有同学认为应该在长颈漏斗内放置浸有稀硫酸的棉花团,其目的是 。
(5)关闭K 2停止通入NH 3,还要继续通入一段时间CO 2,其目的是 。
(6)写出副产品氯化铵和熟石灰反应的化学方程式 。