工业上利用生产钛白的副产品硫酸亚铁制备还原铁粉的流程如图
(1)“转化”时在溶液中生成了FeCO3沉淀,从四种基本反应类型来看,该反应的类型是 ;“过滤”后得到的滤液中的溶质有 (填化学式)
(2)“干燥”过程中有少量的FeCO3转化为FeOOH和CO2,此时与FeCO3反应的物质有 (填化学式);FeCO3和FeOOH在空气中焙烧转化为Fe2O3,写出Fe2O3在高温条件下与C反应生成Fe和CO2的化学方程式 。
(3)制得的还原铁粉中含有Fe和少量FexC.为确定FexC的化学式,进行了如下实验:
①取14.06g还原铁粉在氧气流中充分加热,得到0.22g CO2;
②另取相同质量的还原铁粉与足量稀硫酸充分反应(FexC与稀硫酸不反应),得到0.48g H2.FexC的化学式是 。
小峰和小刚阅读试剂标签后发现,市场销售的高锰酸钾晶体纯度高达99.5%,含水量可以忽略不计,为探究“试管放置方式对高锰酸钾制取氧气速度和体积的影响”,他俩设计了制取氧气的直立型装置(如图),并与斜卧型装置比较,在气密性良好的装置中分别加入5.0克高锰酸钾晶体,用同一酒精灯 分别加热,用同一型号的集气瓶收集气体,每组实验进行五次,实验数据取平均值后记录如下表:
|
装置类型 |
直立型 |
斜卧型 |
|
收集1瓶氧气所需时间/秒 |
59 |
68 |
|
收集2瓶氧气所需时间/秒 |
95 |
108 |
|
收集氧气的总体积/毫升 |
525 |
476 |
(1)收集2瓶氧气,所需时间较短的装置类型是 ;
(2)等质量的高锰酸钾加热到不再产生气体,斜卧型装置收集到氧气的总体积比直立型少的原因是 ;
(3)根据2KMnO4 K2MnO4+MnO2+O2↑,算出5.0克高锰酸钾生成的氧气体积为理论值。实验中发现,斜卧型发生装置收集到的氧气体积明显大于理论值,他们对其原因进行了探究:
K2MnO4+MnO2+O2↑,算出5.0克高锰酸钾生成的氧气体积为理论值。实验中发现,斜卧型发生装置收集到的氧气体积明显大于理论值,他们对其原因进行了探究:
【提出假设】
小峰假设:反应生成的二氧化锰在较高温度下受热分解出氧气;
你的假设: 。
【设计实验】要验证小峰的假设能否成立,请设计简明的实验方案 。

海尔蒙特、普利斯特利、萨克斯等多位科学家用了几百年的时间,经过无数次的实验才对光合作用有了比较清楚地认识,有许多关于"验证叶片在光合作用和呼吸作用过程中有气体的产生和消耗"的经典实验流传至今,现将其中一个实验的思路及过程简述如下:
(注:NaHCO 3稀溶液能维持溶液中CO 2浓度恒定.其原理是当CO 2浓度降低时,NaHCO 3稀溶液能释放CO 2,当CO 2浓度升高时,NaHCO 3稀溶液能吸收CO 2.)
①剪取一烟草叶片,立即将其放入盛有NaHCO 3稀溶液的容器中,发现叶片浮于液面;
②用真空泵抽去该叶片中的气体后,发现叶片下沉至容器底部;
③将该容器放在阳光下一段时间,发现叶片逐渐上浮
④再将该容器放在黑暗环境中一段时间,发现叶片又慢慢下沉至容器底部.
请你用所学的知识对以上③、④中叶片的上浮与下沉现象进行解释. 
小苏打(NaHCO3)和食盐NaCl是厨房中常用物质,现有一包白色固体,可能由NaHCO3和NaCl中的一种或两种组成。某科学小组同学展开了系列拓展性研究。
(一)定性分析
【实验目的】确定白色固体的组成
【实验方案】
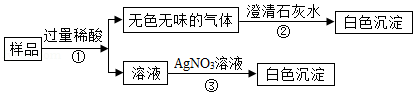
【实验结论】该白色固体 由NaHCO3和NaCl两种物质组成
(1)基于上述实验结论,则步骤①中加入的过量稀酸应该是
(2)写出步骤②中生成白色沉淀的化学反应方程式
(二)定量分析
【实验目的】测定该白色固体中NaHCO3的质量分数
为了测定该样品中NaHCO3的质量分数,小吕、小周分别取a克该样品,设计了如下方案:
小吕方案Ⅰ:利用NaHCO3与稀硫酸反应产生CO2,通过测定生成CO2的质量,计算样品中NaHCO3的质量分数
(3)小吕用下列装置完成本实验,装置的连接顺序是 (填装置的字母编号,装置不重复使用);
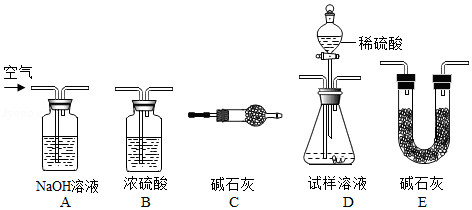
(4)D装置中的反应完全后,需再次通入空气,其目的是
小周方案Ⅱ:小周用沉淀法测定样品中的NaHCO3的质量分数。操作流程如下:
(已知:NaHCO3+NaOH═Na2CO3+H2O)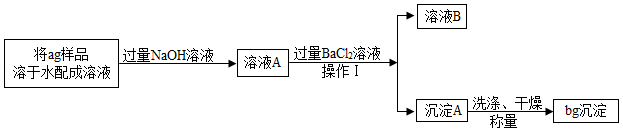
(5)为使定量分析更准确,在操作Ⅰ之前,需判断所加BaCl2溶液是否过量,请你设计一个合理方案: 。
已知某混合气体由H 2、CO和CO 2三种气体组成。为验证该混合气体成分,科学研究小组的同学经过讨论,设计了如图1所示的实验方案。

根据方案回答下列问题:
(1)装置C在实验中的作用是
(2)仅根据D装置中黑色粉末变红这一现象,能否证明混合气体中一定存在CO?请判断并说明理由
(3)小丁根据装置E中出现白色硫酸铜粉末变成蓝色的实验现象,得出该混合气体中有氢气存在的结论。你认为结论是否可靠?若可靠,请说明理由;若不可靠,请对图1实验装置提出改进意见
(4)图1方案B装置可用来吸收CO 2但没有现象。为证明CO 2和NaOH能发生反应,小丁又设计了图2所示的方案。则图2方案中所加试剂X应该是 。
人体代谢产生的过氧化氢,对人体有毒害作用。人体肝脏中的过氧化氢酶能催化过氧化氢分解产生氧气和水。某同学查阅资料发现,FeCl3也能通过催化过氧化氢分解。为比较过氧化氢酶和FeCl3催化效率的高低,该同学在28℃环境下进行了如下探究:
(1)提出问题:过氧化氢酶和FeCl3催化效率哪个更高?
(2)猜想与假设:
(3)实验材料:适宜浓度的FeCl3溶液,适宜浓度的新鲜猪肝研磨液(含有过氧化氢酶),适宜浓度的过氧化氢溶液等。
(4)实验步骤:
①取2支洁净的试管,编号为1、2,并各注入3mL适宜浓度的过氧化氢溶液;
②向1号试管内滴入2滴适宜浓度的FeCl3溶液,向2号试管内 ;
③观察并记录两支试管产生气泡的情况。
(5)预测实验结果:
请写出一种可能的实验结果:
(6)在以上探究的基础上,该同学又完成了“探究温度对猪肝研磨液和FeCl3催化效率的影响”实验。实验结果如图所示。图中代表猪肝研磨液催化效率的曲线是 ,判断的理由是 。
