海螵蛸是一味中药,其主要成分是碳酸钙,某同学利用如图装置测定其中碳酸钙的含量。
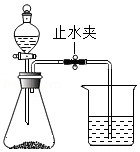
①在锥形瓶中加入质量为m的海螵蛸粉末,向分液漏斗中加入稀盐酸。在烧杯中加入足量氢氧化钠溶液,并称量烧杯及氢氧化钠溶液总质量m 1。
②先打开止水夹,再打开分液漏斗活塞,滴加盐酸并及时关闭活塞。完全反应后,再次称量烧杯及其中液体的总质量m 2。
③利用m 2与m 1的差值,计算反应生成的二氧化碳质量,再计算海螵蛸中碳酸钙的含量。
(1)海螵蛸具有治疗胃酸过多、能为骨质发育提供重要元素的功效,其原因是 。
(2)实验前要检查装置的气密性,方法是:用止水夹夹住橡胶管,往分液漏斗中加入适量水。打开分液漏斗的活塞,观察到 ,说明装置气密性良好。
(3)下列情况会导致海螵蛸中碳酸钙质量分数测量值偏小的是 (可多选)。
A.海螵蛸中滴加盐酸过量
B,锥形瓶内部分水蒸气随二氧化碳逸出
C.反应结束后,锥形瓶内有二氧化碳残留
D.反应速度过快,大量气泡从氢氧化钠溶液中溢出
(1)向24.5g氯酸钾中加入少量二氧化锰,加热、充分反应后,生成氯化钾14.9g。则生成氧气的质量是 g,该反应的化学方程式是 。
(2)向盛有一定量硝酸银溶液的试管中加入14.9g氯化钾,恰好完全反应,过滤,得到120.2g滤液,求该硝酸银溶液的质量(写出计算步骤)
如图一是某食品标签,小颖看到食品添加剂中有“碳酸氢铵”,感觉很惊讶,“碳酸氢铵”是臭粉啊,怎么可以放进食品?于是开展了以下探究,请你帮助完成下列相关问题。
(1)分析食品成分:营养物质:配料中含有多种营养物质,其中富含糖类的有 ;
食品添加剂:主要是盐类,酸类等物质。
(2)查阅资料:①食用级碳酸氢铵比较纯净,可作膨松剂,一般用在油炸食品中,水蒸食品中不用;
②常温常压下,1体积水约能溶解600体积氨气,其水溶液呈弱碱性。
(3)产生疑惑:臭粉为何可以作膨松剂?为何一般适用于油炸食品而不适用于水蒸食品?
(4)实验设计:实验装置如图,图二是检验装置,图三是收集装置,取适量碳酸氢铵分别置于两试管中,按如图进行实验。
(5)现象与分析:①图二:反应过程中的现象是 ,C中澄清石灰水变浑浊,当B中不再有气泡冒出时,A装置试管中固体消失、 。
②图三:装置E的作用是 ,F中收集到氨气,说明氨气具有 性质,取下F,塞上橡皮塞,用注射器向F中注入少量水,看到的现象是 ,拔出橡皮塞闻到氨味。
(6)解释与结论:①有臭味的碳酸氢铵添加到食品中,如果油炸,则含有的少量碳酸氢铵受热时完全分解,产生的气体使食品膨胀,且生成物可以迅速挥发而离开食品,没有残留物,其臭味会消失,碳酸氢铵发生反应的化学方程式是
②添加碳酸氢铵的食品如果水蒸,则 。
通过上述探究小颖明白了:高纯度的碳酸氢铵可以作为食品添加剂,但同一食品添加剂并不适合所有食品,使用食品添加剂需严格控制用量。


某化学学习小组在实验室做了一次探究活动,以下是该小组填写的探究报告。
|
探究内容 |
探究铝分别与稀盐酸、稀硫酸的反应 |
|
知识应用 |
根据金属活动性顺序表,铝能与酸反应 |
|
实验准备 |
用同样的标准打磨大小、厚薄相同的2片铝 |
|
进行实验 |
室温时,向盛有等量稀盐酸、稀硫酸的2支试管中加入打磨光亮的相同的2片铝 |
|
现象描述 |
铝与稀盐酸反应速率很快,产生大量气泡;铝与稀硫酸反应速率一直很慢,几乎看不到气泡 |
|
分析猜想 |
铝分别与稀盐酸、稀硫酸分反应现象为什么相差甚远?猜想如下:①铝片表面氧化铝的影响;②铝片表面积的影响;③反应时外界温度的影响; ④硫酸铝难溶于水,阻碍了铝与稀硫酸的反应;⑤两种酸的氢离子浓度不同;⑥稀盐酸中含有的Cl﹣加快了铝和稀盐酸的反应;⑦稀硫酸中含有的SO42﹣阻碍了铝和稀硫酸的反应 |
请仔细阅读探究报告,回答下列问题
(1)猜想④不合理,理由是
(2)经过分析可以排除其影响因素的猜想有 (填序号)
(3)选择一个你认为合理的猜想并设计实验进行验证,你选择的合理猜想的序号是 ,实验设计是:室温时,将打磨光亮的相同的2片铝分别放入2支试管中,再 ,观察现象。
请根据如图回答相关问题

(1)A中称量某固体时选用砝码的顺序是 ,如该固体是NaOH则不能用滤纸垫在托盘上进行称量,原因是 。
(2)B操作有错误,正确的操作是 。
(3)C中细铁丝在氧气中反应的化学方程式是 ,将细铁丝拧成螺旋状的目的是 。
(4)用双氧水与二氧化锰制氧气时发生装置可选D,该装置还可用于制 等气体。
钢是铁的合金。为测定某钢样中铁的质量分数,取11.4g钢样,向其中加入稀硫酸,产生氢气的质量与加入稀硫酸的质量关系如图所示(不考虑钢样中其它成分与稀硫酸的反应)。
(1)钢 (填“是”或“不是”)金属材料。
(2)计算此钢样中铁的质量分数。
