我国著名化学家侯德榜先生发明了“侯氏制碱法”,其原理中重要的一步是向饱和食盐水中先后通入足量NH3和CO2制备NaHCO3,化学方程式:NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl
某兴趣小组在实验室模拟该过程,请结合具体的步骤回答下列问题: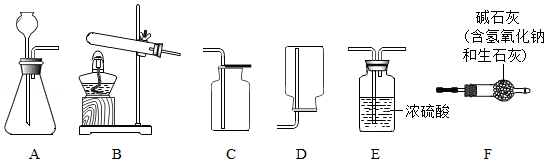
I.气体制备
(1)二氧化碳气体制备
实验室常采用石灰石与稀盐酸反应制备CO2,其化学方程式为 。应选择的气体收集装置为 (选填装置对应的字母)。
(2)氨气制备
实验室常用硫酸吸收氨气,防止污染空气,实验室制备NH3的反应原理为:Ca(OH)2(固)+2NH4Cl(固) CaCl2+2H2O+2NH3↑.现要制备并干燥NH3,所选装置的正确连接顺序为 → (选择装置对应的字母)。实验室制备O2也可用上述制备NH3的发生装置,写出用该发生装置制备O2的化学方程式 。
II.NaHCO3制备
物质 |
NaHCO3 |
NH4Cl |
溶解度/g(20℃) |
9.6 |
37.2 |
(3)根据表格中的溶解度数据,解释20℃产物中NaHCO3能够先从溶液中结晶析出的原因 。
(4)该过程中另一产物NH4Cl在农业生产中常被用作 。
科学家尝试通过多种途径减少CO 2的排放,或将CO 2转化为有用的物质。其中一种途径是利用NaOH溶液来"捕捉"CO 2,并将CO 2储存或利用,反应流程如图所示。

(1)反应分离室中分离物质的操作是 。
(2)上述反应流程中,可循环利用的物质是 。
(3)若反应分离室中有溶质质量分数为10.6%的Na 2CO 3溶液100千克,求完全反应后,理论上可生成CaCO 3的质量(要求根据化学方程式计算)。
饮食关系着人们的健康,许多人喜欢吃油炸食品,经检测,这些食品中含致癌物质﹣丙烯酰胺(C 3H 5NO)。
(1)丙烯酰胺属于 (填"无机物"或"有机物")
(2)丙烯酰胺中各元素的质量比C:H:N:O= 。
为测定CuCl 2和FeCl 2组成的混合溶液中FeCl 2的质量分数,进行如下实验:
①取200g混合溶液加入足量的AgNO 3溶液,经过滤、洗涤、干燥、称量,得到143.5g AgCl固体;
②另取原混合溶液各200g与含有杂质的废铁屑反应(杂质不溶于水,也不参与反应),共做了五组实验,其实验数据如下表。
|
实验组别 |
一 |
二 |
三 |
四 |
五 |
|
混合溶液质量/g |
200 |
200 |
200 |
200 |
200 |
|
铁屑质量/g |
6 |
9 |
12 |
15 |
18 |
|
析出铜的质量/g |
6.4 |
9.6 |
m |
16 |
16 |
请分析计算:
(1)表中第三组实验的m值为 。
(2)第 组实验恰好完全反应。
(3)铁屑中铁的质量分数为多少?(计算结果精确到0.1%)
(4)原混合溶液中FeCl 2的质量分数为多少?(计算结果精确到0.1%)
丁酸乙酯是无色有菠萝香味的液体,其密度为0.87g/cm 3,难溶于水,可与油类互溶。现取11.6g丁酸乙酯在氧气中完全燃烧,只产生26.4gCO 2和10.8gH 2O。
(1)含有丁酸乙酯的物品应远离火源。若丁酸乙酯燃烧, (填"能"或不能")用水来灭火。
(2)丁酸乙酯可与油类互溶,这种性质属于 性质。
(3)丁酸乙酯中碳元素和氢元素的质量比为 。
某拓展性学习小组在学校科学实验创新比赛中,做了一个有趣的实验,装置如图。
实验设计:三颈烧瓶中充满二氧化碳气体,A颈、B颈分别连接充满氢氧化钠溶液和盐酸的注射器,C颈插有两端开口的玻璃导管(伸入瓶内的一端连有小气球),装置气密性良好。
实验操作:先通过A颈往瓶内注入氢氧化钠溶液,观察到小气球的形状发生了变化;过一段时间后再通过B颈往瓶中注入盐酸,发现小气球的形状又发生了改变。
请描述小气球形状的变化情况,并对此作出合理的解释。
