苯佐卡因是临床常用的一种手术用药。以甲苯为起始原料的合成路线如图。

回答问题:
(1)甲苯分子内共面的H原子数最多为 个。
(2)A的名称是 。
(3)在A的同分异构体中,符合下列条件的是 ( 写出一种结构简式)。
①与A具有相同官能团
②属于芳香化合物
③核磁共振氢谱有5组峰
(4)B中官能团名称为 。
(5)B→C的反应方程式为 。
(6)反应过程中产出的铁泥属于危化品,处理方式为 ( 填编号)。
a.高温炉焚烧
b.填埋
c.交有资质单位处理
(7)设计以甲苯和丙三醇为原料合成3﹣苄氧基﹣1,2﹣丙二醇(  )的路线 (其他试剂任选)。
)的路线 (其他试剂任选)。
已知:在于HCl催化下丙酮与醇ROH反应生成缩酮。缩酮在碱性条件下稳定。在酸中水解为丙酮和醇ROH。
水杨酸甲酯又叫冬青油,是一种重要的有机合成原料。某化学小组用水杨酸(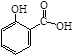 )和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率。
)和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率。
实验步骤:
Ⅰ.如图,在三颈烧瓶中加入6.9 g (0.05 mol)水杨酸和24 g(30 mL,0.75 mol)甲醇,向混合物中加入约10 mL甲苯(甲苯与水形成的共沸物,沸点为85℃,该实验中加入甲苯,易将水蒸出),再小心地加入5 mL浓硫酸,摇动混匀,加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时:
Ⅱ.待装置冷却后,分离出甲醇,然后转移至分液漏斗,依次用少量水、5%NaHCO3溶液和水洗涤;分出的产物加入少量无水MgSO4固体,过滤得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221℃~224℃的馏分,得水杨酸甲酯4.5g。
常用物理常数:
| 名称 |
分子量 |
颜色状态 |
相对密度 |
熔点(℃) |
沸点(℃) |
| 水杨酸甲酯 |
152 |
无色液体 |
1.18 |
-8.6 |
224 |
| 水杨酸 |
138 |
白色晶体 |
1.44 |
158 |
210 |
| 甲醇 |
32 |
无色液体 |
0.792 |
-97 |
64.7 |
请根据以上信息回答下列问题:
(1)仪器A的名称是,制备水杨酸甲酯时,最合适的加热方法是。
(2)实验中加入甲苯对合成水杨酸甲酯的作用是。
(3)反应结束后,分离甲醇的操作是。
(4)洗涤操作中,第一次水洗的主要目的是,第二次水洗的主要目的是。
(5)检验产品中是否含有水杨酸的化学方法是。
(6)本实验的产率为___________(保留两位有效数字)。
.实验探究:为了研究同周期元素性质递变规律,某同学自己设计了一套实验方案,并动手记录实验步骤和现象如下:(表中的“实验步骤”与“实验现象”前后不一定是对应关系)
| 实验步骤 |
实验现象 |
| ① 将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 |
A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色。 |
| ②在盛有冷水的烧杯中滴入几滴酚酞溶液,再将一小块金属钠放入其中 |
B.有气体产生,溶液变成浅红色 |
| ③将镁条投入稀盐酸中 |
C.剧烈反应,迅速产生大量无色气体 |
| ④将铝条投入稀盐酸中 |
D.反应不十分剧烈;产生无色气体。 |
| ⑤向A1Cl3溶液中滴加NaOH溶液至过量 |
E.生成白色胶状沉淀,继而沉淀消失 |
请你帮助该同学整理并完成实验报告:
(1)实验用品:试剂:金属钠、镁条、铝条、稀盐酸、AlC13溶液、NaOH溶液、酚酞溶液等。
实验所用到的玻璃仪器:①、②、③以及胶头滴管、玻璃片等。
(2)实验内容:(填写与实验步骤对应的实验现象的编号和②的化学方程式)
| 实验内容 |
① |
② |
③ |
④ |
⑤ |
| 实验现象(填A~F) |
B |
(3)此实验的结论:钠、镁、铝的金属性强弱。
某化学课外小组用右图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。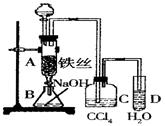
(1)写出A中反应的化学方程式______________________________;
(2)观察到D中的现象是______________________________;
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是____________,写出有关的化学方程式______________________________;
(4)C中盛放CCl4的作用是______________________________。
(5)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入_______,现象是__________________。
氢化锂(LiH)在干燥的空气中能稳定存在,遇水或酸能够引起燃烧。某活动小组准备使用下列装置制备LiH固体。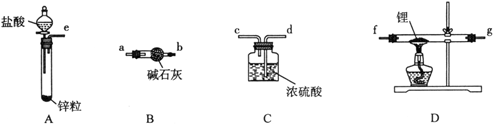
甲同学的实验方案如下:
(1)仪器的组装连接:上述仪器装置接口的连接顺序为____________________,加入药品前首先要进行的实验操作是__________(不必写出具体的操作方法);其中装置B的作用是______________。
(2)添加药品:用镊子从试剂瓶中取出一定量金属锂(固体石蜡密封),然后在甲苯中浸洗数次,该操作的目的是________________________________________,然后快速把锂放入到石英管中。
(3)通入一段时间氢气后加热石英管,在加热D处的石英管之前,必须进行的实验操作________。
(4)加热一段时间后停止加热,继续通氢气冷却,然后取出LiH,装入氮封的瓶里,保存于暗处。采取上述操作的目的是为了避免LiH与空气中的水蒸气接触而发生危险。(反应方程式:LiH + H2O =" LiOH" + H2↑),分析该反应原理,完成LiH与无水乙醇反应的化学方程式______________________________________。
(5)准确称量制得的产品0.174g,在一定条件下与足量水反应后,共收集到气体470.4 mL(已换算成标准状况),则产品中LiH与Li的物质的量之比为____________________。
(6)乙同学对甲的实验方案提出质疑,他认为未反应的H2不能直接排放,所以在最后连接了装置E用来收集H2,请将E装置补充完整。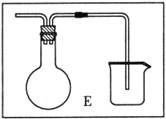
二氧化氯( ClO2)是一种极易爆炸的强氧化性气体,在生产和使用时必须尽量用“隋性”气体进行稀释,并尽可能防止震动和避光。因此,二氧化氯的制备方法一直是科学家长期寻求解决的问题,目前比较理想的方法是用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得。已知,ClO2在常温下是一种黄绿色有刺激性气味的气体,其熔点为一59℃,沸点为11.0℃,易溶于水。某学生拟用图1所示装置模拟工业制取并收集ClO2.
(1)A中反应产物有K2CO3、ClO2和CO2等,请写出该反应的化学方程式:。A装置必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有烧杯、。
(2)B装置必须放在冰水浴中,其原因是。
(3)反应后在装置C中可得NaClO2溶液。已知(1)NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2.3H2O,在温度高于38℃时析出晶体是NaClO2,温度高于60℃时NaClO2分解生成NaClO3和NaCl;NaClO2的溶解度曲线如图2所示,请补充从NaClO2溶液中制得NaClO2晶体的操作步骤:
①减压,55℃蒸发结晶;②;③;④低于60℃干燥;得到成品。
(4)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:量取ClO2溶液10 mL,稀释成100 mL试样。
步骤2:量取V1 mL试样加入到锥形瓶中,调节试样的pH≤2.0,加入足量的Ⅺ晶体,摇匀,在暗处静置30 min。
步骤3:以淀粉溶液作指示剂,用c mol∙L-1 Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL。(已知I2+2S2O32- =2I- +S4O62-)
①若步骤2中未将锥形瓶“在暗处静置30min”,立即进行步骤3,则测定的结果可能(选填“偏大”、“偏小”或“无影响”)。
②上述步骤3中滴定终点的现象是。
③根据上述步骤可计算出原ClO2溶液的浓度为g-L一1,(用含字母的代数式表示)。