如图所示,600K时,在容积可变的透明容器内,反应2HI(气) I2(气)+H2(气)达到平衡状态A。保持温度不变,将容器的容积压缩成为原容积的一半,达到平衡状态B。按图示观察方向__▲__(填“能”或“不能”)看出两次平衡时容器内颜色深浅的变化,理由是_▲__。若从水平方向观察,能否看到容器内颜色深浅的变化__▲___。
I2(气)+H2(气)达到平衡状态A。保持温度不变,将容器的容积压缩成为原容积的一半,达到平衡状态B。按图示观察方向__▲__(填“能”或“不能”)看出两次平衡时容器内颜色深浅的变化,理由是_▲__。若从水平方向观察,能否看到容器内颜色深浅的变化__▲___。
通常用小苏打的悬浊液除去CO2中的HCl,该反应的离子方程式为,不能用NaOH溶液的原因是_____________,也不能用NaCO3的原因是_____________________(用离子方程式表示原因)。
(8分)填写下列空白:
(1)写出表示含有8个质子、10个中子的原子的原子符号:________。
(2)周期表中位于第8纵行的铁元素属于第________族。
(3)周期表中最活泼的非金属元素位于第________纵行。
(4)所含元素超过18种的周期是第______________周期。
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所
处的周期序数与主族序数相等,请回答下列问题:
(1)T元素的离子结构示意图为__________。
(2)元素的非金属性(原子得电子的能力):Q ________W(填“强于”或“弱于”)。
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,该反应的化学方程式为_________________________________________
(4)原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是_________________________________________________________其反应物的电子式为。离子半径T3+__________R3-(填“>”、“<”、“=”)
(5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2 L的甲气体与0.5 L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐只有一种,则该含氧酸盐的化学式是____________。
已知A、B、C、D四种短周期元素在元素周期表中的相对位置如下图所示,它们的原子序数之和为46。请填空: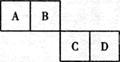
(1)B元素的名称为D元素的原子结构示意图为。
(2)B有多种氧化物,其中之一是一种无色气体。该气体在空气中会迅速变成红棕色,在一定条件下,4L的该无色气体与3L的氧气相混合,被足量的水完成吸收,且只生成一种B的含氧酸,该含氧酸的化学式为。
(3)离子半径:D﹣C2﹣(填“>”、“<”、“=”)。
还原性:D﹣C2﹣(填“>”、“<”、“=”)。
(9分)某非金属单质A经如下图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题:
(1)若A常温下为淡黄色固体,B是有刺激性气味的无色气体。
①A、D的化学式分别为:AD
②工业生产中大量排放的B气体被雨水吸收后形成而污染环境。
③写出B→C反应的化学方程式:
(2)若A在常温下为气体,C是红棕色气体。
①A的电子式为,C的化学式为
②写出C→D反应的化学方程式: