研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学方程式为 ;利用反应6NO2+ 8NH3 7N5+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
7N5+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
(2)已知:2SO2(g)+O2(g) 2SO3(g)
2SO3(g)
ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g) 2NO2(g)
2NO2(g)
ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH= kJ·mol-1。一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
SO3(g)+NO(g)的ΔH= kJ·mol-1。一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 molNO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K= 。
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图所示。该反应ΔH 0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图所示。该反应ΔH 0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
【化学——选修3:物质结构与性质】
已知A、B、C、D、E是元素周期表中1~36号元素,其原子序数依次增大,且A、B、C、D为主族元素。A与另外四种元素既不在同一周期,也不在同一主族。B和C同主族,D和E同周期;元素E是周期表中的第7列元素,D的最外层电子数与最内层电子数相同,D跟B可形成离子化合物,其晶胞结构(其中B原子在晶胞内部)如图。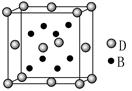
请回答下列问题:
(1)C-的电子排布式为______________;E元素原子的价电子排布式为________。
(2)元素B与氮元素可以形成化合物NB3,其中N—B键的化学键类型为________,根据价层电子对互斥理论可以判断NB3的空间构型为________,NB3分子中N原子的杂化方式为________杂化。
(3)A、B形成的化合物AB的相对分子质量比A、C形成的化合物AC的相对分子质量小,但AB的沸点比AC高,其原因是。
(4)从晶胞图可以得出:D与B形成的离子化合物的化学式为。
(5)含有D元素的化合物焰色反应为______色,焰色反应的原理是。
(共10分)有机物A为烃类化合物,质谱图表明其相对分子质量为70,其相关反应如下图所示,其中B、D、E的结构中均含有2个—CH3,它们的核磁共振氢谱中均出现4个峰。请回答:
(1)D的分子式为;
(2)E中所含官能团的名称为;
(3)Ⅲ的反应类型为(填字母序号);
a.还原反应 b.加成反应 c.氧化反应 d.消去反应
(4)C和E可在一定条件下反应生成F,F为有香味的有机化合物,该反应的化学方程式为
;
(5)A的同分异构体中有一对互为顺反异构,且结构中有2个—CH3,它们的结构简式为和
;
(6)E有多种同分异构体,其中一种同分异构体能发生银镜反应,能与足量金属钠生成氢气,不能发生消去反应,其结构简式为。
乙酸苯甲酯( )是有香味的有机化合物,它可以从茉莉花中提取,也可
)是有香味的有机化合物,它可以从茉莉花中提取,也可
以用甲苯和乙醇为原料进行人工合成。一种合成路线如下:

(1)C的名称为。
(2)写出反应①的化学方程式:。
(3)反应③的反应类型为。
(4)反应(填序号)原子的理论利用率为100%,符合绿色化学的要求。
完成下列空白。
(1)“辛烷值”用来表示汽油的质量,汽油中异辛烷的爆震程度最小,将其辛烷值标定为100下图
是异辛烷的球棍模型,则异辛烷的系统命名为。
(2)写出下列反应的化学方程式:
① 2,5-二甲基-2,4-己二烯与足量氢气加成:;
② 2-甲基-2-丁烯加聚反应 ;
③ 甲苯在一定条件下生成三硝基甲苯:;
(3)烯烃与溴化氢、水加成时,产物有主次之分,例如:
CH2==CHCH3+HBr→CH3CHBrCH3 (主要产物) + CH3CH2CH2Br(次要产物)
A是一种不对称烯烃,与HBr加成时,生成的主要产物为B,且B中仅含有4个碳原子、1个溴原子、1种氢原子。则B的结构简式为,A的结构简式为。
现有:
| A.CH3OH | B.(CH3)3CCH2OH | C.(CH3)3COH | D.(CH3)2CHOH E. C6H5CH2OH 五种 |
有机物。(填字母序号)
(1)能氧化成醛的是。
(2)不能消去成烯烃的是。
(3)能氧化成酮的是。
(4)E与甲酸发生酯化反应的产物是(写结构简式)。