Cl2O为国际公认高效安全灭菌消毒剂之一,它是棕黄色强刺激性气体,沸点3.8℃熔点-116℃。实验室可用潮湿的Cl2与Na2CO3反应制取少量Cl2O,装置如下(图Ⅰ):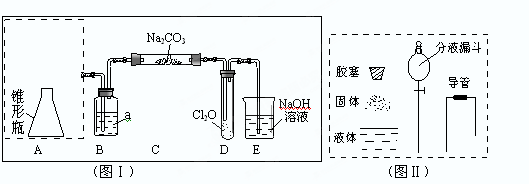
回答下列问题:
(1)把浓盐酸直接滴在KMnO4晶体上就可以产生Cl2。请模仿“图Ⅱ”在“图Ⅰ”A处补画出正确的装置图,并作必要的标注。
(2)B中试剂a应选用 (填下列序号字母):
a.CCl4 b.饱和NaCl溶液 c.浓H2SO4 d.饱和NaHCO3溶液
(3)通入适量的氯气,在C中生成棕黄色的物质Cl2O,该物质常温下为气体,方程式为:
Cl2+ Na2CO3+ = NaHCO3+ NaCl+ Cl2O
(4)对C中反应后的固体成分进行检验,请写出实验步骤以及预期的现象和结论。限选实验试剂和仪器:蒸馏水、稀HNO3、BaCl2溶液、Ba(OH)2溶液、AgNO3溶液、澄清石灰水、试管、小烧杯、带导管的橡皮塞、过滤装置。
| 实验步骤 |
现象和结论 |
| 步骤一:取C中的少量固体样品于试管中,滴加足量蒸馏水至完全溶解,然后将溶液分别置于a、b试管中。 |
|
| 步骤二:向a试管中滴加BaCl2溶液,静置。 |
无明显现象,证明固体中不含Na2CO3 |
| 步骤三: |
|
| 步骤四: |
则证明固体中含有NaCl。 |
某小组同学用下图装置进行实验研究(a、b、c表示止水夹)。请评价或完善其方案: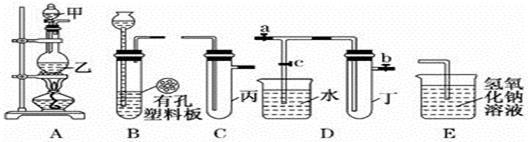
(1)将装置A、C、E相连接,用MnO2和浓盐酸制取氯气,请回答:
①A中反应的离子方程式:_ 。
②E中氢氧化钠溶液的作用 。在C中加入适量的水可制得氯水.将所得氯水分成两份进行实验,其操作、现象和结论为:
| 实验序号 |
实验操作 |
现象 |
结论 |
| Ⅰ |
将氯水滴入品红溶液 |
品红溶液褪色 |
氯气有漂白性 |
| Ⅱ |
氯水中加入碳酸氢钠粉末 |
有无色气泡产生 |
氯气与水反应的产物具有酸性 |
③实验Ⅰ推出的相应结论是否合理?________,若不合理,请说明理由(若合理,无需填写)____________。
④实验Ⅱ推出相应的结论是否合理?_______,若不合理,请说明理由(若合理,无需填写)_____________。
(2)将B、D、E相连,在B中装浓硝酸和铜片,可制得NO2并进行有关实验。
①B中反应的化学方程式________________________。
②先若关闭c,当丁中充满红棕色的NO2时,再关闭止水夹a、b ,微热试管丁,丁中可观察到的实验现象 。
某课外活动小组模拟工业制备纯碱,方案如下:
(一)实验原理:NaCl+H2O+NH3+CO2═NaHCO3↓+NH4Cl
向饱和食盐水中通入足量氨气至饱和,然后通入二氧化碳,析出溶解度较小的碳酸氢钠.
(二)实验装置:所需实验药品和装置如图所示:
(三)实验步骤
(1)搭好装置,然后应该进行的操作是__________。
(2)中间的烧瓶中加入20mL饱和食盐水,并将其浸入冰水中;D中加入足量氢氧化钠固体,E中加入足量浓氨水;B中加入足量碳酸钙粉末,A中加入足量稀硫酸于(可分多次加入).仪器A的名称是__________,选择用稀硫酸而不用稀盐酸的好处是__________。
(3)先打开__________(填K1或K2),将装置A或E中的试剂慢慢加入圆底烧瓶,烧瓶中产生气体的原理是__________,大约20分钟左右时,观察到饱和食盐水上方有__________大量的白雾
现象时,再打开__________(填K1或K2),将装置A或E中的试剂慢慢加入圆底烧瓶,大约5分钟即有浑浊出现,约15分钟出现大量白色固体.
(四)纯碱制备:
(4)上述实验结束后,欲得到纯碱,将固体过滤、洗涤后,还需进行的操作是__________(不加任何其它试剂,装置任选),反应的化学方程式为__________;若将上述操作产生的气体全部通过浓硫酸,再通过足量的过氧化钠,过氧化钠增重0.28g,则制得的纯碱质量为__________g。
掌握物质之间的转化,是学习元素化合物知识的基础。
(1)中学常见的某反应的化学方程式为:A+B→C+D+H2O(未配平,反应条件略去)。
若C、D均为气体,且都能使澄清石灰水变浑浊。
①请写出该反应的化学方程式 ;
②某探究性学习小组利用图中所列装置实验,证明上述反应中有C、D生成。则a瓶对应的现象是 ,b瓶溶液还可以用 代替。
③装置d中所盛溶液是 。
(2)为研究硝酸置于适量的浓HNO3和稀HNO3中(如下图所示)。
①气球的作用是 。
②A中,最终溶液变为浅绿色,发生反应的离子方程式是 。
③B中,无明显变化,该同学进一步探究如下:
假设:Ⅰ常温下铁与浓硝酸不反应。
Ⅱ 。
进行实验,将B中的铁片取出并洗净后,放入CuSO4溶液中,无明显变化,则说明假设Ⅰ (填“成立”或“不成立”)。
长途运输鱼苗时,人们常在水中加入少量过氧化钙(CaO2)固体。甲、乙两位同学发现往水中投入过氧化钙时产生气泡。
【查阅资料】CaO2与Na2O2具有相似的化学性质。
【提出问题】当CaO2投入足量水中时,最终会生成什么物质呢?
【进行猜想】甲同学认为,生成氧化钙和氧气;乙同学认为,生成氢氧化钙和氧气。
(1)甲同学的猜想明显是错误的,其理由是________________________。
(2)写出乙同学猜想发生反应的化学方程式________________________。
【实验验证】
(3)一同学设计如下实验:取少量CaO2放入试管中,加足量水充分反应,待没有气体逸出时,滴加几滴_____________,观察到溶液变红,则证明有氢氧化钙生成。乙同学发现红色很快褪去了。他通过查阅资料了解到还生成了一种曾经学习过的物质,请你猜测该物质是_____________。
(4)请你利用如图所示装置设计实验予以证明。
X中CaO2与水充分反应后的溶液,Y中的固体物质为__________________。打开分液漏斗活塞,使X中溶液滴下,_________(补充完后续试验的操作、现象),则证明你的猜测合理。
某学习小组研究“不同条件对化学反应速率影响的探究”,选用4 mL 0.01 mol·L-1KMnO4溶液与2 mL 0.1 mol·L-1 H2C2O4溶液在稀硫酸中进行实验,改变条件如表:
| 组别 |
草酸的体积 /mL |
温度/℃ |
其它物质 |
| ① |
2 mL |
20 |
|
| ② |
2 mL |
20 |
2滴饱和MnSO4溶液 |
| ③ |
2 mL |
30 |
|
| ④ |
1 mL |
20 |
1 mL蒸馏水 |
(1)如果研究催化剂对化学反应速率的影响,使用实验 和 (用 ①~④表示,下同);如果研究温度对化学反应速率的影响,使用实验 和 。
(2)对比实验①和④,可以研究 对化学反应速率的影响,实验④中加入1 mL蒸馏水的目的是 。