Ⅰ.铁是一种过渡元素,金属铁是最常用的金属之一。请回答下列问题:
(1)生铁中含有一种铁碳化合物(Fe3C),在足量的空气中高温煅烧,生成有磁性的固体和能使澄清石灰水变浑浊的气体,该反应的化学方程式为 ,上述反应生成的磁性固体与过量浓硝酸反应后的溶液中含有的盐的化学式为 。
(2)硫酸厂用煅烧黄铁矿(FeS2)来制取硫酸,实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2)制备绿矾。利用烧渣制绿矾的过程如下: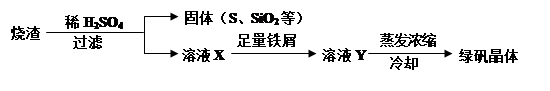
①烧渣溶于稀H2SO4过程中,有单质硫生成,写出该反应的离子方程式(只写生成S的反应式,其他反应无需写出) 。
②向溶液X中加入足量铁屑的目的是 。
(3)已知Fe(OH)3的溶度积常数Ksp=1.1×10-36。室温时向FeCl3溶液中滴加NaOH溶液,当溶液pH=3时,通过计算说明Fe3+是否沉淀完全)
(提示:当某离子浓度小于10-5 mol•L-1时可以认为该离子沉淀完全了)。
Ⅱ.(1)某溶液中有Mg2+、Fe3+、Al3+、Cu2+等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入到过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的金属阳离子是________;用离子方程式解释其原因_________________。
(2)在25℃下,向浓度均为0.01 mol・L-1的MgCl2和AlCl3混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式______________(已知25℃时Ksp[Mg(OH)2]=1.8×10-11 Ksp[Al(OH)3]="3×10" -34)。
(3)将Mg、Cu组成的1.96g混合物投入过量稀硝酸中,充分反应后,固体完全溶解时收集到还原产物NO气体0.896L(标准状况),向反应后的溶液中加入2mol/L的NaOH溶液80mL时金属离子恰好完全沉淀。则形成沉淀的质量为 g。
选择下列某种答案的序号, 填入下表的空格
①同位素②同素异形体③同分异构体④同系物⑤同种物质
| 物质 |
丁烷与 |
红磷 |
氯仿与 |
氕与 |
新戊烷与 |
| 名称 |
2--甲基丙烷 |
与白磷 |
三氯甲烷 |
氘、氚 |
2,2--二甲基丁烷 |
| 相互 |
|||||
| 关系 |
铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
(1)Cu位于元素周期表第I B族。Cu2+的核外电子排布式为 ▲。
(2)右图是铜的某种氧化物的晶胞结构示意图,可确定该晶胞中阴离子的个数为 ▲。
(3)胆矾CuSO4·5H2O可写成[Cu(H2O)4]SO4·H2O,其结构示意图如下: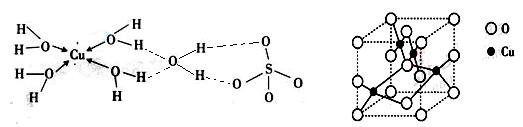
下列说法正确的是 ▲(填字母)。
| A.在上述结构示意图中,所有氧原子都采用sp3杂化 |
| B.在上述结构示意图中,存在配位键、共价键和离子键 |
| C.胆矾是分子晶体,分子间存在氢键 |
| D.胆矾中的水在不同温度下会分步失去 |
(4)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是 ▲。
酞菁也是常见的配位体,结构如右图。该分子中氮原子杂化方式为 ▲。 写出与硫酸根离子互为等电子体的分子和离子各一种 ▲、 ▲。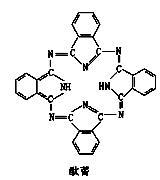
(5)Cu2O的熔点比Cu2S的 ▲(填“高”或“低”),
请解释原因 ▲。
硫酸钙是一种用途非常广泛的产品。
(1)25℃时,Ksp(CaSO4)=7.10×10-5。在1L0.1mol·L-1CaCl2溶液中加入1L0.2mol·L-1的Na2SO4溶液,充分反应后(假设混合后溶液的体积变化忽略不计)溶液中Ca2+物质的量的浓度为 ▲mol·L-1。
(2)某校课外活动小组为测定已部分脱水的生石膏的组成(xCaSO4·yH2O),做如下实验:将固体放在坩埚中加热,经测量剩余固体质量随时间变化如图所示。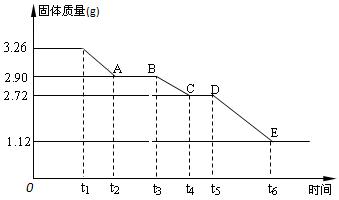
①x :y =____▲_____。
②② t2~t3时间段固体的化学式为 ▲。
③ t5~t6时间段固体质量减轻的原因是产生了两种气体,其中一种能使品红溶液褪色,则该时间段所发生反应的化学方程式为。
异噁草酮是一种色素抑制类除草剂,它的工业合成路线如下: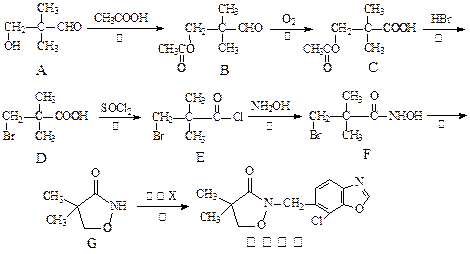
⑴从A→D过程中,反应①的目的是 ▲。
⑵写出满足下列条件的A的一种同分异构体的结构简式 ▲。
①与A具有相同的官能团;②分子中具有两个手性碳原子。
⑶物质D与NaOH溶液反应的化学方程式为 ▲。
⑷由G制备异噁草酮的反应中要加入试剂X(C8H5NOCl2),X的结构简式为 ▲。
⑸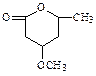 是B的一种重要的同分异构体。请设计合理方案,完成从
是B的一种重要的同分异构体。请设计合理方案,完成从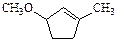 到
到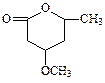 的合成路线(用合成路线流程图表示,并注明反应条件)。
的合成路线(用合成路线流程图表示,并注明反应条件)。
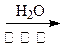 ……
……
提示:①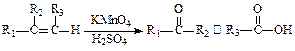 ;
;
②合成过程中无机试剂任选;
③合成路线流程图示例如下:
CH3CH2OH CH2=CH2
CH2=CH2
 CH2-CH2
CH2-CH2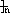
纳米TiO2作为一种光催化剂越来越受到人们的关注,现正广泛开发运用。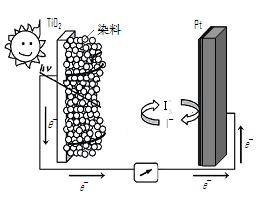
(1)制取纳米TiO2的方法很多,氢氧火焰水解法是将TiCl4气体导入氢氧火焰中(700~1000℃)进行水解,其化学反应式为: ▲。
(2)纳米二氧化钛可光解挥发性有机污染物(VOCs),若无水蒸气存在,三氯乙烯降解反应为:C2HCl3+2O2→2CO2+HCl+Cl2,若有足够量的降解后的尾气,实验室检验产物中有氯气的简单方法是:▲;通过质谱仪发现还有多种副反物,其中之一为: ,则该有机物核磁共振氢谱有 ▲ 个峰。
,则该有机物核磁共振氢谱有 ▲ 个峰。
(3)利用半导材料TiO2与染料、铂电极及I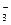 和I-的混合物作电解质(I2+I-
和I-的混合物作电解质(I2+I- I
I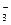 ),可构成染料敏化太阳能电池(DSSCs)工作原理如右图,该电池工作时,正极的电极反应为:▲。
),可构成染料敏化太阳能电池(DSSCs)工作原理如右图,该电池工作时,正极的电极反应为:▲。
(4)在不同的载体(钛片、铝片、陶瓷)表面制备二氧化钛薄膜,来考察不同载体TiO2薄膜光催化使甲基橙脱色,每次光照20min取一次样,实验结果如下。 w ww.k s5u. co m
w ww.k s5u. co m
下列说法正确的是 ▲。
(a)不同载体,无论何种温度一定是钛片最好
(b)约在520℃时,钛片载体的光催化活性最好
(c)无论何种载体,催化活性总是随温度的升高而升高
(d)不同负载TiO2薄膜的光催化活性不同