我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法。
I.已知:2CO(g)+ O2(g)=2CO2(g),ΔH=-566 kJ·mol-1
2Fe(s)+  O2(g)=Fe2O3(s),ΔH=-825.5 kJ·mol-1
O2(g)=Fe2O3(s),ΔH=-825.5 kJ·mol-1
则CO还原Fe2O3反应的热化学方程式为: 。
Ⅱ.反应  Fe2O3(s)+ CO(g)
Fe2O3(s)+ CO(g)
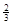 Fe(s)+ CO2(g)在1000℃的平衡常数等于4。在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过l0min后达到平衡。
Fe(s)+ CO2(g)在1000℃的平衡常数等于4。在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过l0min后达到平衡。
(1)反应到10min时,用CO2表示该反应的速率为 ,CO的平衡转化率=____________,平衡后再分别加入Fe、Fe2O3、CO、CO2各0.4mol,则正反应速率 逆反应速率(填“大于”、“小于”或“等于”)。
(2)欲提高CO的平衡转化率,促进Fe2O3的转化,可采取的措施是________.
a.降低反应温度
b.增大反应体系的压强
c.选取合适的催化剂
d.及时吸收或移出部分CO2
e.粉碎矿石,使其与平衡混合气体充分接触
Ⅲ.高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:
CO(g)+2H2(g) CH3OH(g),请根据图示回答下列问题:
CH3OH(g),请根据图示回答下列问题:
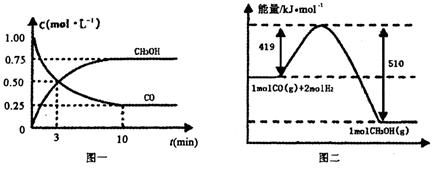
(1)若在温度和容器相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡吋的有关数据如下表:
| 容器 |
反应物投入的量 |
反应物的 转化率 |
CH3OH的浓度 |
能量变化 (Q1、Q2、Q3均大于0) |
| 甲 |
1molCO和2molH2 |
α1 |
c1 |
放出Q1kJ热量 |
| 乙 |
1molCH3OH |
α2 |
c2 |
吸收Q2kJ热量 |
| 丙 |
2molCO和4molH2 |
α3 |
c3 |
放出Q3kJ热量 |
则下列关系正确的是________.
A.c1=c2
B.2Q1=Q3
C.2a1=a3
D.a1+a2=1
E.该反应若生成1molCH3OH,则放出(Q1+Q2)kJ热量
(2)若在一体积可变的密闭容器中充入lmolCO、2molH2和1molCH3OH,达到平衡吋测得混合气体的密度是同温同压下起始的1.6倍,则该反应向________(填“正”、“逆”)反应方向移动。
(3)甲醇可与氧气构成燃料电池,该电池用多孔的惰性电极浸入浓氢氧化钾溶液,写出该电池的负极反应式______________________,若电解质溶液为酸性,写出正极反应式_________________。
(本题共12分)
23.铁与同周期的钙性质有很大的差异,铁的熔点更高,而钙的金属活动性更强,这都说明铁的金属键比钙更_____(选填“强”、“弱”)。与钢铁比,纯净的铁有很强的抗腐蚀性,原因____________________。氯化铁受热会发生升华现象这说明氯化铁是______________(选填“离子”、“共价”)化合物。
24.一定条件下,在容积一定的容器中,铁和CO2发生反应:Fe(s)+CO2(g) FeO(s)+CO(g),该反应的平衡常数表达式K=__________。下列措施中能使平衡时c(CO)/c(CO2)增大的是___________(选填编号)。
FeO(s)+CO(g),该反应的平衡常数表达式K=__________。下列措施中能使平衡时c(CO)/c(CO2)增大的是___________(选填编号)。
a.升高温度b.增大压强 c.充入一定量COd.再加入一些铁粉
25.S2可在Fe2(SO4)3溶液中“溶解”,硫元素都以SO42-形式存在,请完成该反应的化学方程式。
______FeS2+______Fe2(SO4)3+___ _________→_____FeSO4+_____ __________
26.溶液的酸碱性对许多物质的氧化性有很大影响;生成物的溶解性会影响复分解反应的方向。将Na2S溶液滴加到FeCl3溶液中,有单质硫生成;将FeC13溶液滴加到Na2S溶液中生成的是Fe2S3而不是S或Fe(OH)3
从以上反应可得出的结论是______________________、_______________________________。
(本题共12分)CuSO4∙5H2O是铜的重要化合物,有着广泛的应用。以下是CuSO4∙5H2O的实验室制备流程圈。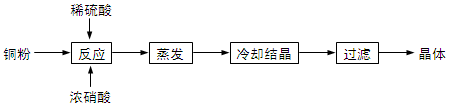
根据题意完成下列填空:
41、向含铜粉的稀硫酸中滴加少量浓硝酸(可加热),在铜粉溶解时可以观察到的实验现象:。
42、根据反应原理,硝酸与硫酸的理论配比(物质的量之比)为。
43、已知:CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4
称取0.1000g提纯后的CuSO4∙5H2O试样于锥形瓶中,加入0.1000mol/L氢氧化钠溶液28.00mL,反应完全后,过量的氢氧化钠用0.1000mol/L盐酸滴定至终点,耗用盐酸20.16mL,则0.1000g该试样中含CuSO4∙5H2Og。
44、在滴定中,眼睛应注视;滴定终点时,准确读数应该是滴定管上蓝线所对应的刻度。
45、若上述滴定操作中,滴定管加盐酸之前未进行润洗,则测得试样中所含CuSO4∙5H2O的质量(填“偏大”“偏小”或“无影响”)。
46、如果l.040g提纯后的试样中含CuSO4∙5H2O的准确值为1.015g,而实验测定结果是1.000g,测定的相对误差为。
(本题共12分)CO的应用和治理是当今社会的热点问题。
29、CO能导致镍系催化剂中毒,工业上常用SO2除去原料气中少量CO,生成物为固体S和CO2。
写出该反应的化学方程式为。
30、上述反应中,每减少2.24L气体(标准状况下),转移电子数为。
CO工业上可用于高炉炼铁,发生如下反应: Fe2O3(s) + CO(g)
Fe2O3(s) + CO(g)
 Fe(s) + CO2(g),
Fe(s) + CO2(g),
已知该反应在不同温度下的平衡常数如下表:
| 温度/℃ |
1000 |
1150 |
1300 |
| 平衡常数 |
4.0 |
3.7 |
3.5 |
31、下列说法不正确的是(选填序号)
a.该反应是一个放热反应
b.该反应的平衡常数表达式是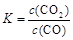
c.其他条件不变,向平衡体系充入CO2气体,K值减小
d.当K值等于1时,反应达到平衡
32、欲提高CO的平衡转化率,促进Fe2O3的转化,可采取的措施是(选填序号)
a.及时吸收或移出CO2 b.增大反应体系的压强
c.用更高效的催化剂 d.粉碎矿石,增大接触面积
高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:CO(g) + 2H2(g) CH3OH(g) + Q
CH3OH(g) + Q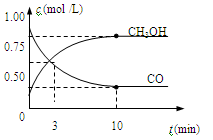
33、从上图可以看出,反应开始到平衡,反应速率v(H2)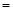 。
。
34、甲醇氧化可生成甲酸,能使0.1mol/L的甲酸溶液的电离度与pH值都增大的是(选填序号)。 a.加水稀释 b.加入少量甲酸钠固体
a.加水稀释 b.加入少量甲酸钠固体
c.通氯化氢 d.加入少量苛性钠固体
(本题共12分)元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
23、第三周期元素的原子所形成的简单离子中:还原性最弱的阴离子是;氧化性最强的阳离子是。
24、下列事实可以作为S和Cl非金属性强弱的判断依据的是(选填序号)
a.Cl的最高正价比S高b.可用浓H2SO4制HCl
c.HCl的酸性比H2S强d.Cl2与H2S反应生成S
25、硅元素最外层有种能量不同的电子;SiCl4的空间构型和CH4相同,写出SiCl4的电子式:。
26、PH3和NH3的某些化学性质相似。下列对晶体PH4I性质的推测,错误的是(选填序号)
a.PH4I是一种共价化合物b.PH4I能与烧碱溶液反应
c.PH4I加热后会发生升华 d.PH4I溶液能与溴水反应
27、二氯化二硫(S2C12)可用作橡胶工业的硫化剂,它的分子结构与H2O2相似。下列有关说法不正确的是(选填序号)
a.S 2C12分子中有4对共用电子对
b.S2C12分子中没有非极性键
c.S2C12分子中,S为+1价,Cl为-1价
d.S2C12分子中各原子均为8电子稳定结构
28、已知NaHSO3溶液显酸性,溶液中存在以下平衡:
HSO3-+H2O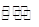 H2SO3+OH- ①
H2SO3+OH- ①
HSO3-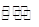 H++SO32- ②
H++SO32- ②
向0.1mol/L的NaHSO3溶液中加入少量氢氧化钠固体,则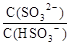 (填“增
(填“增
大”“减小”或“不变”,后同),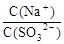 。
。
(化学——物质结构与性质,13分)下面的表格是元素周期表的一部分,其中的字母对应不同的元素。
| A |
||||||||||||||||||
| M |
Q |
R |
||||||||||||||||
| E |
D |
|||||||||||||||||
| G |
J |
|||||||||||||||||
请回答下列问题:
(1)G和J形成的合金是一种贮氢材料,其晶体结构与氯化铯相同。该合金中每个G原子周围与其最近且等距的J原子有个。该晶体属于晶体
A.离子晶体 B.原子晶体 C.分子晶体 D.金属晶体
(2)M3R2是一种直线型分子R=M=M=M=R,该分子是一种分子(填极性或非极性)。
(3)请写出D-的电子排布式:。
(4)M2A2也是直线型分子,1个分子中含有个σ键。
(5)化合物E2D6分子中各原子均达到了八电子稳定结构,请画出其结构式(用元素符号表示)。