(1)汽车排气管内安装的催化转化器,可使尾气中主要污染物(NO和CO)转化为无毒的大气循环物质。已知:
①N2(g)+O2(g)="2NO(g)" ΔH=+180.5 kJ·mol-1
②2C(s)+O2(g)="2CO(g)" ΔH=-221.0 kJ·mol-1
③C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
则该反应的热化学方程式为:________________。
(2)NO2与SO2混合可发生反应:NO2+SO2 SO3+NO。
SO3+NO。
I.在100℃1molNO2与1molSO2的混合气体置于绝热恒容密闭容器中发生上述反应,
①正反应速率随时间变化的趋势如图所示,则下列说法正确的是___________(填字母)。

| A.反应在c点达到平衡状态 |
| B.反应物浓度:a点小于b点 |
| C.反应物的总能量高于生成物的总能量 |
| D.△t1=△t2时,SO2的消耗量:a~b段大于b~c段 |
E.当反应达到平衡时,继续充入1molNO2,则NO的体积分数变小
②判断此反应达到平衡的标志是_______
A 体系的压强不再发生变化
B 混合气体的密度不变
C 混合气体的平均相对分子质量不变
D 各组分的物质的量浓度不再改变
E 体系的温度不再发生变化
F v(NO2)正=v(NO)逆
II.在常温时,维持体系总压强P恒定,体积为V升的1molNO2与1molSO2的混合气体于密闭容器发生上述反应,已知NO2的平衡转化率为α,则在该温度下反应的平衡常数K=_____________(用α,V等符号表示)。
(3)熔融盐燃料电池具有较高的发电效率,因而受到重视。某燃料电池以熔融的K2CO3(其中不含O2-和HCO3-)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极。试回答下列问题:
①该燃料电池正极电极反应式为:______________。
②25℃时,某学生想用该燃料电池电解一定量的硫酸钠饱和溶液中进行电解,当电路中有amol电子转移时,溶液中析出mgNa2SO4·10H2O晶体。若温度不变,在剩余溶液中溶质的质量分数为__________,消耗掉的丁烷在标准状况下的体积为______________。
氮化硅(氮显-3价,硅显+4价)是一种高温陶瓷材料,它的硬度大、熔点高、化学性质稳定,工业上曾普遍采用高纯硅与纯氮在1300 ℃时反应获得。
(1)写出N的原子结构示意图________和氮化硅的化学式________。
(2)氮化硅陶瓷抗腐蚀能力强,除氢氟酸外,它不与其他无机酸反应。试推测该陶瓷被氢氟酸腐蚀的化学方程式____________________________。
(3)现用四氯化硅和氮气在氢气气氛保护下,加强热发生反应,可得较高纯度的氮化硅,反应的化学方程式为_____________________。
为测定一种气态烃A的化学式,取标准状况下一定体积的A置于密闭容器中,再通入一定体积的O2 ,用电火花引燃,定性实验表明产物是CO2、CO、水蒸气。相关方案及有关数据如下(图中的箭头表示气体的流向,实验前系统内的空气已排除)。
试回答:
(1)通过计算求出A的实验式(最简式)。
(2)根据所学知识,你认为气态烃A只能是哪种物质?你的根据是什么?
已知:①A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2 2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
回答下列问题:
(1)、写出A的电子式。
(2)B、D分子中的官能团名称分别是、。
(3)写出下列反应的反应类型:①,②,④。
(4)写出下列反应的化学方程式:
①;
② ;
④。
(5)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图。请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法。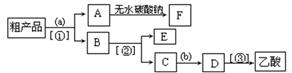
(Ⅰ)试剂a是__________,试剂b是_______________;
分离方法①是_________________,分离方法②是__________________,
分离方法③是_______________。
(Ⅱ)在得到的A中加入无水碳酸钠粉末,振荡,目的是
______。
(Ⅲ)写出C → D 反应的化学方程式 。
已知X、Y、Z都是短周期元素,它们的原子序数依次递增,X原子的电子层数与它的核外电子总数相同,而Z原子的最外层电子数是次外层电子数的三倍,Y和Z可以形成两种以上的气态化合物,则
(1)写出下列元素名称:X是________,Z是________。
(2)由Y和Z组成,且Y和Z的质量比为7∶20的化合物的分子式是________。
(3)写出由X、Y、Z中的两种元素组成,且与X2Z分子具有相同电子数的两种阴、阳离子_______和_______,其中阴离子的电子式为______________。
(4)X、Y、Z可以形成一种盐,此盐中X、Y、Z元素的原子个数比为4∶2∶3,该盐的化学式是_______________;如果向该盐溶液中加入铜和稀硫酸,溶液变蓝色,试写出离子方程式_____ __;如果将该盐固体与熟石灰混合加热,会产生一种刺激性气味的气体,试写出化学方程式__________________________________。
在下列各组物质中,找出合适的序号填在对应的空格内:
①NO2和N2O4 ②12C和14C ③ 和
和 
④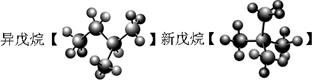

⑥甲烷与丙烷 ⑦乙醇(CH3CH2OH)和乙二醇(HO—CH2—CH2—OH)
注意:以上七组物质,不一定是每组物质都能找到对应填空
⑴互为同位素的是 ;⑵互为同分异构体的是 ;
⑶互为同系物的是 ;⑷同一种物质的是 。