今年5月,运用"蓝鲸一号"钻探平台,我国南海神狐海域首次实现可燃冰试采成功.
材料一:可燃冰、学名天然气水化合物,其化学式为CH 4•8H 2O.它是天然气的固体状态(因海底高压).埋于海底地层深处的大量有机质在细菌的分解作用下,最后形成石油和天然气(石油气),其中许多天然气被包进水分子中,在海底的低温(2~5℃)与压力下结晶,形成"可燃冰".
材料二:"蓝鲸一号"钻探平台设计和建造过程刷新了多项世界纪录,它长117米,宽92.7米,高118米,质量为42000吨.
请根据上述材料回答:
(1)形成可燃冰需要一定的生态环境.
①海底地层深处,这些分解有机质的细菌能很好的生存,体现了生物对环境的 .这些细菌分解有机质 (选填"需要"或"不需要")氧气,这些细菌与真菌在细胞结构上的主要区别是 .
②在开采过程中,极少量的垃圾废弃物没有对海洋环境造成破坏,这主要是因为海洋生态系统有 的能力.
(2)形成可燃冰的其中一个条件是有甲烷气源.
①可燃冰(CH 4•8H 2O)中C:H:O的元素质量比是 ,甲烷属于 (选填"有机物"或"无机物").
②与石油、煤等化石燃料相比较,开采可燃冰的积极意义有(写一条) .(可燃冰在空气中燃烧的化学方程式为CH 4•8H 2O+2O 2  CO 2+10H 2O)
CO 2+10H 2O)
(3)如果南海海水的密度是1.03×10 3千克/米 3,"蓝鲸一号"钻探平台漂浮海面受到海水浮力是 牛,浸入海水的体积至少需要 米 3,开采出的可燃冰可以直接在管口点燃,说明已经成为气体,从固体变成气体的原因可能是 .
请阅读下面的材料,回答有关问题。
研究显示:每年排放的二氧化碳近一半存留在大气层,其它被陆地和海洋吸收。人类大量使用煤、石油和天然气等化石燃料,砍伐森林,导致过量的二氧化碳进入海洋,使海洋酸化,表层海水平均pH从8.1下降到7.9。人类给海洋的二氧化碳越多,海水pH越小,吸收二氧化碳的能力就会相对减弱,这样的循环会导致海洋生物链发生变化。
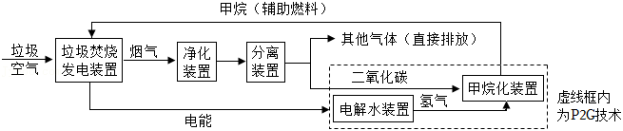
垃圾焚烧发电是生活垃圾处理的有效方式之一,但垃圾焚烧会产生烟尘和有害气体,还会增加二氧化碳的排放,加剧海洋酸化;同时垃圾焚烧需要购买辅助燃料,成本较高。我国烟气处理协同P2G技术很好地解决了这些问题,其主要流程如图所示。
(1)过量的二氧化碳进入海洋,使海洋酸化,发生反应的化学方程式为 。
(2)下列有关海洋酸化的说法不正确的是 (选填字母序号)。
| A. |
海洋酸化是指表层海水呈酸性 |
| B. |
海洋酸化会导致气候变暖加剧 |
| C. |
海洋酸化不会影响海洋生物及其生态系统 |
| D. |
海洋酸化会改变海水中某些离子的浓度 |
(3)流程中“净化装置”的作用是 ,“其它气体”的主要成分有O2和 (填化学式)等气体。
(4)使用P2G技术的优点是 (写一条即可)。
(5)“甲烷化装置”中发生的化学反应是 ,其中X是 (填化学式)。
(6)若用P2G技术处理550kg二氧化碳,使其完全反应。请根据化学方程式计算生成甲烷的质量(写出计算过程)。
(1)某化学小组的同学对金属元素及金属材料进行系列研究。
①人类文明进步与金属材料的发展关系十分密切。常见的金属材料有铁合金、铜合金、铝合金,这三种合金被广泛应用的年代由远及近的正确排列顺序是下列选项中的 (填选项序号之一)。
| A. |
铜合金→铁合金→铝合金 |
| B. |
铁合金→铝合金→铜合金 |
| C. |
铝合金→铜合金→铁合金 |
②我国劳动人民很早就掌握了湿法冶金的技术,西汉的《淮南万毕术》、东汉的《神农本草经》都有用单质铁置换出铜盐中铜的记载,试写出用单质铁与 溶液反应进行湿法炼铜的化学方程式: 。
③黄铜是由铜和锌所组成的合金,其外观与黄金非常相似。将黄铜置于稀盐酸中,能观察到的明显现象是 (写出一条即可)。
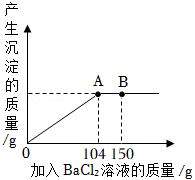
(2)现有 和 的固体混合物10g,将其全部放入一洁净的烧杯中,然后加入足量蒸馏水,搅拌,使固体完全溶解。再向烧杯中逐滴加入溶质质量分数为10%的 溶液,反应过程中产生沉淀的质量与所滴入 溶液的质量关系如图所示。试回答:
①当滴入 溶液150g时(即图中B点),烧杯中溶液里存在的酸根阴离子是 (填离子符号)。
②当滴入 溶液104g时(即图中A点),恰好完全反应,试通过计算,求10g该固体混合物中 的质量。(计算结果精确至0.1g)
科学探究是认识和解决化学问题的重要实践活动。
近年来,自热食品种类繁多。只需将撕去塑料膜的发热包放入凉水中,就能享用美食,很受年轻人的追捧。实验小组同学买来一份自热食品进行以下探究。
【资料】Ⅰ.发热包中物质的主要成分是生石灰、碳酸钠、铝粒。
Ⅱ.铝能和 溶液反应生成偏铝酸钠( )和氢气,偏铝酸钠溶于水。
探究一:发热包的发热原理。
(1)小组同学取出发热包,撕去塑料膜,放入适量凉水中,可观察到的现象是 ,固体迅速膨胀,同时还可观察到发热包内固体变硬结块,其可能的原因是 (用化学方程式表示)。
(2)在使用发热包过程中,禁止明火的理由是 。
探究二:反应后混合物中部分成分的探究。

根据以上操作和实验现象回答下列问题。
(3)操作Ⅰ的名称是 。
(4)根据现象①得出:滤液A中一定不含的物质是 。根据现象②③分析得出:固体B中一定含有的物质是 。综合分析得出:现象③中产生的气体,其成分的组成可能为 。
(5)通过以上探究,同学们进行反思总结,你认为其中正确的是 。
| A. |
能与水混合放出热量的物质均可做发热包的发热材料 |
| B. |
发热包应密封防潮保存 |
| C. |
禁止用湿手接触发热包 |
| D. |
使用过程中应保持通风 |
科学探究离不开实验活动。

(1)仪器a的名称是 。
(2)实验室用加热高锰酸钾的方法制取氧气,并用于进行铁丝在氧气中燃烧的实验,最好选用的发生装置和收集装置是 。
(3)向装置A中加入少量氧化铜作催化剂,再向其中加入68g过氧化氢溶液,反应结束后,共产生1.6g氧气,写出该反应的化学方程式 ,所用过氧化氢溶液的溶质质量分数为 。
(4)实验小组同学用石灰石和6%的稀盐酸制取 时,发现固体仍有大量剩余,但不再产生气泡,请写出一种可能的原因 ,并设计实验进行验证 。
(5)以下反应均可生成 (极易溶于水,密度比空气小):
①
②
③
结合以上装置,适合作为实验室制取 的反应原理有 (填序号)。
从古至今,铁及其化合物一直被人类广泛应用。
(一)铁及其化合物的应用

(1)明代科学著作《天工开物》中记载:
①“其器冶铁锥,其尖使极刚利”,“铁锥”为开挖盐井的工具。所取盐井水“入于釜中煎炼顷刻结盐”,“金”指生铁制作的铁锅。生铁属于 材料。上述描述中利用铁的 (选填序号)。
| A. |
a.导热性 |
| B. |
b.导电性 |
| C. |
c.硬度大 |
②“泥固塞其孔,然后使水转釉”是指高温下 将红砖中的
将红砖中的 转化为
转化为 而形成青砖。该转化的化学方程式为 。
而形成青砖。该转化的化学方程式为 。
(2)铁的化合物在现代更多领域发挥着重要作用。
①碳酸亚铁( )不溶于水,可作补血剂,服用后与胃酸反应生成 被人体吸收,促进血红蛋白的生成。
)不溶于水,可作补血剂,服用后与胃酸反应生成 被人体吸收,促进血红蛋白的生成。
②火星探测器发回的信息表明,火星上存在 ,从而证明火星表面曾经存在过水,其理由为 。
,从而证明火星表面曾经存在过水,其理由为 。
③活性 可除去石油开采过程中的有害气体
可除去石油开采过程中的有害气体 ,并获得
,并获得 ,原理如下。
,原理如下。

吸收中生成的另一种物质的化学式为 ,再生时发生反应的化学方程式为 。
(二) 的制备
的制备
用废铁屑(主要成分为 ,含少量
,含少量 和
和 )制备
)制备 主要流程如下。
主要流程如下。

(1)酸溶时适当提高反应温度和 浓度,目的是 ,产生的气体为 。
浓度,目的是 ,产生的气体为 。
(2)还原发生的反应为 。
。
沉淀发生的反应为 。
。
沉淀时反应温度不宜太高,原因是 。
(3)沉淀时会有部分 与
与 反应生成
反应生成 ,反应的化学方程式为 。
,反应的化学方程式为 。
(三) 的含量测定
的含量测定
已知: 及铁的氧化物加热分解的温度如下。
及铁的氧化物加热分解的温度如下。

称取含 的
的 样品76.6g,进行热分解实验。控制不同的温度对样品加热,测得剩余固体质量随温度的变化如图所示。
样品76.6g,进行热分解实验。控制不同的温度对样品加热,测得剩余固体质量随温度的变化如图所示。

(1)样品中 的含量为 %(精确到0.1%)。
的含量为 %(精确到0.1%)。
(2)当加热到 时,M点固体的成分是 ,对应的质量比为 。
时,M点固体的成分是 ,对应的质量比为 。